Startschuss zu MedTech Connect: Klinische Prüfungen in der Medizintechnik

DATUM
25. März 2021
AUTOR
Kristina Weber | Product Lead
Diese Woche fand unser erstes #MedTechConnect Event statt und wir haben uns riesig gefreut, so viele Teilnehmer aus der Medizintechnik-Branche dabei zu haben! Rund 75 Gäste fanden am 24. März um 16 Uhr im Online-Meetup zusammen, um über klinische Prüfungen für Medizinproduktehersteller zu diskutieren.
Worum ging’s?
Woher weiß ich als Hersteller, ob und wann ich eine klinische Prüfung benötige? Und welche Art von klinischer Prüfung muss es dementsprechend sein? Welche typischen Herausforderungen erwarten mich in diesem Zusammenhang und wie gehe ich am besten damit um?
Diese und weitere Fragen stellen sich zahlreiche Medizinproduktehersteller, egal ob sie vor ihrer allerersten klinischen Studie stehen oder Daten über bereits inverkehrgebrachte Produkte erheben müssen.
In diesem informellen Meet-up haben Climedo Health, Curedatis und eye2you neben zwei spannenden Impulsvorträgen einen Raum geboten, um konkreten Erfahrungen und Problemstellungen mitzubringen und sich mit anderen Herstellern und Experten zu vernetzen.
Wer waren die Referenten?
Neben Veronika Schweighart, die das Event moderierte, waren Robert Radloff von Curedatis sowie Dr. Jörn-Philipp Lies von eye2you mit dabei.
Als Mitgründerin von Climedo Health begleitet Veronika Schweighart Kunden aus der Medizintechnik auf ihrem Weg zur erfolgreichen elektronischen Datenerhebung im Rahmen von klinischen Studien und PMCF.
Robert Radloff ist Biologe und ehemaliger klinischer Monitor für Arzneimittel- und Medizinproduktestudien. Als Gründer von Curedatis unterstützt er Medizinprodukte- und DiGA-Hersteller auf ihrem Weg zur automatisierten Evidenzsynthese.
Philipp Lies ist Neurowissenschaftler und ehemaliger Berater. Er arbeitet seit über 2 Jahren mit seinem Startup eye2you an der Vision, unnötige Erblindungen weltweit zu verhindern. Sie entwickeln dafür eine Smartphone-Software als Medizinprodukt der Klasse IIa
Impulsvortrag 1: “Wann ist eine klinische Prüfung bei Medizinprodukten notwendig?”
Nach einer kurzen Intro von Veronika Schweighart zeigte Robert Radloff anhand von konkreten Beispielen auf, welche Fragen man sich als Hersteller stellen sollte, wenn man eine klinische Prüfung benötigt bzw. herausfinden will, ob eine Prüfung überhaupt notwendig ist. Hier einige der Leitfragen, die Herstellern bei der Einschätzung helfen:
- Welcher Risikoklasse ist das Produkt zugeordnet?
- Welchen Innovationsgrad weist es auf?
- Gibt es vorhandene klinische Evidenz zum Produkt oder eines gleichartigen Produkts?
- In welcher Entwicklungsstadium- und Regulierungsstatus befindet sich das Produkt?
- Sind offene Fragen und Restrisiken beim Produkt vorhanden?
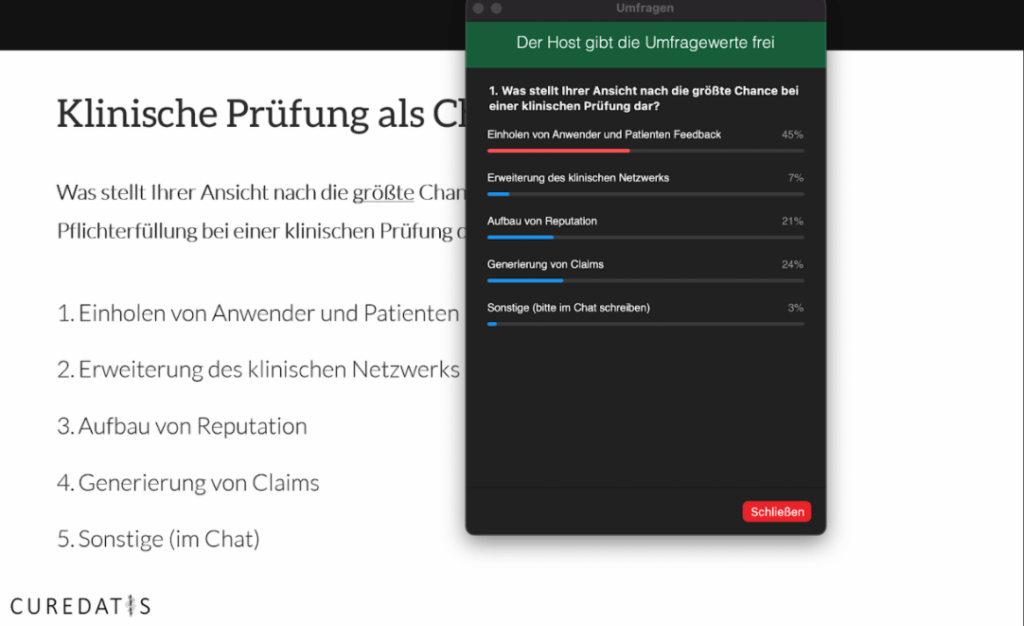
In einer Live-Umfrage hat Robert Radloff die Teilnehmer gefragt, was ihrer Meinung nach neben der regulatorischen Pflichterfüllung die größte Chance bei klinischen Studien sei. Hier eine Übersicht der Auswertung:
An erster Stelle wurde “Einholen von Anwender- und Patienten- Feedback” (45%) genannt, gefolgt von “Generierung von Claims” (24%) an zweiter Stelle und “Aufbau von Reputation (21%) an dritter Stelle.
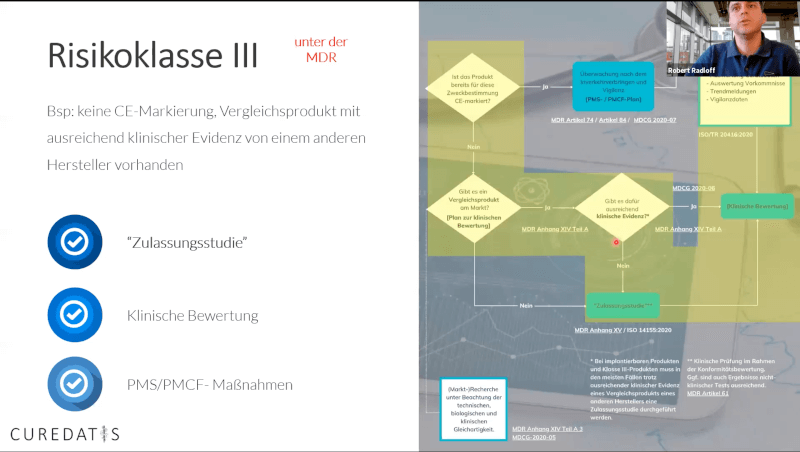
Mithilfe eines neuen Flowcharts spielte Robert Radloff danach konkrete Szenarien und Entscheidungswege für unterschiedliche Produktklassen durch. Das vollständige Flowchart wird in Kürze veröffentlicht.
Vortrag 2: “Herausforderungen zur Durchführung klinischer Studien – ein Praxisbeispiel“
Darauf folgte der zweite Impulsvortrag von Jörn-Philipp Lies. Als Hersteller eines Klasse-IIa-Software-Produkts steht eye2you diversen Herausforderungen gegenüber.
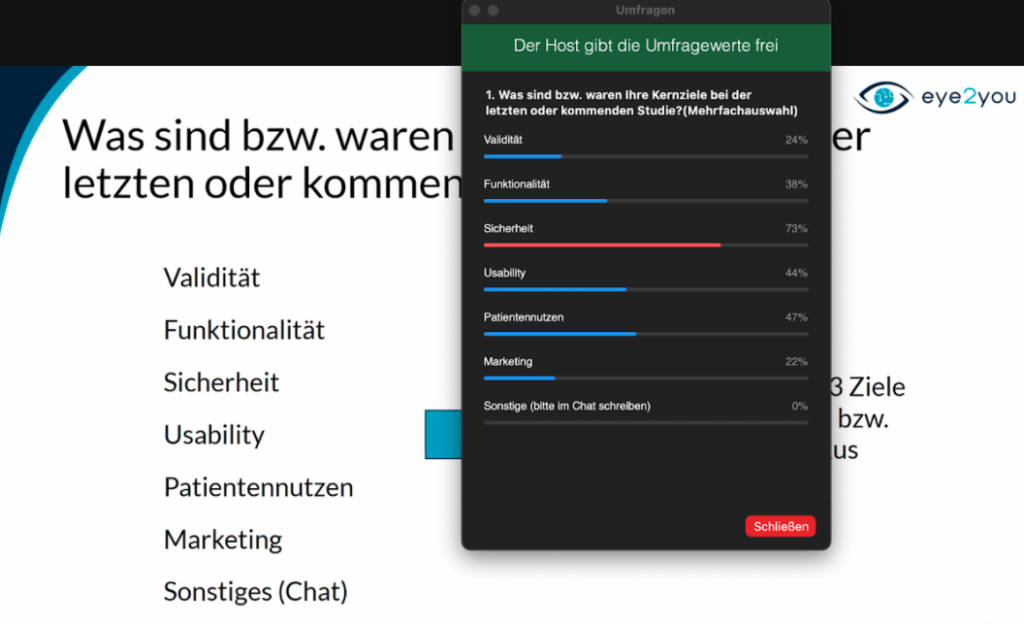
Philipp Lies erklärte, wie durch die Digitalisierung immer mehr Lösungen aus der IT und nicht direkt aus der Medizin stammen und das Bewusstsein für klinische Studien in vielen Fällen erst einmal entwickelt werden muss. Zudem betonte er, dass man sich früh über die Ziele der Studie im Klaren sein muss. Zu den verschiedenen Zielen können zählen:
- Validität: Klappt unsere Idee überhaupt; die Qualität ist hier zunächst nebensächlich
- Funktionalität: Leisten wir das, was wir wollen? Sind wir besser als die Konkurrenz
- Sicherheit: Könnte das Produkt eine Gefahr für Patientïnnen und Anwenderïnnen darstellen?
- Usability: Ist die Nutzung intuitiv und schützt vor Fehlverwendung?
- Patientennutzen: Wie viel besser geht es den Patienten durch unsere Lösung (speziell DiGa)?
- Marketing: Kundïnnen (Ärztïnnen, Patientïnnen, Krankenkassen, …) überzeugen
Diese Frage wurde an das Publikum gestellt, welches “Sicherheit” an erster Stelle sah, wenn es um die Kernziele einer klinischen Prüfung geht.
Im nächsten Schritt, sobald eine Entscheidung über die Art der notwendigen Studie gefallen ist, sollten die Kosten abgeschätzt, Partner identifiziert und Patienten für die Prüfung gefunden werden.
Zum Schluss erläuterte Philipp Lies ein paar Tipps aus der Praxis:
- Vorhandene Evidenz nutzen um Studien effizient zu planen
- Partner finden, die bereit sind, für wissenschaftliche Ergebnisse ihre Zeit und Ressourcen bereitzustellen (Dies gestaltet sich bei modernen Technologien wie SaMD, KI, etc. deutlich einfacher)
- Vernetzung mit anderen Unternehmen
- Studien als wertschöpfenden Teil des Produkts sehen, nicht als bürokratisch-regulatorische Vorgabe
Anschließend gab es zahlreiche Fragen und Impulse aus dem Publikum, auf die unsere Speaker eingingen. Gerne hätten wir noch länger diskutiert, wofür die Zeit allerdings nicht ganz gereicht. Eventuell verlängern wir die Session in Zukunft auf 90 Minuten! 🙂
Vorträge von MedTech Connect als Video-Aufzeichnung ansehen
Wer bei MedTech Connect nicht dabei sein konnte, aber dennoch die Vorträge nachträglich ansehen möchte, kann hier den Link zur Video-Aufzeichnung anfordern.
Speaker gesucht!
Haben Sie auch Lust, mal als Referent an MedTech Connect teilzunehmen? Wir freuen uns, von Ihnen zu hören! Schreiben sie uns eine kurze Nachricht an hello@climedo.de!
Über Curedatis
Curedatis ist ein Start-up, das den Prozess der klinischen Evidenz digitalisiert und automatisiert, um Medizinprodukte-, In-vitro-Diagnostik- und Digital-Health-Unternehmen dabei zu unterstützen, die Anforderungen an eine ausreichende klinische Evidenz gemäß der MDR, IVDR und DiGAV zu erfüllen. Mehr erfahren: www.curedatis.com
Über eye2you
Eye2you ist ein Medizin-KI-Unternehmen das die medizinischen Erstkontakte, wie Hausärzte und Pfleger in die Lage versetzt Untersuchungen der Netzhaut durchzuführen. Dazu benötigen diese lediglich ein handelsübliches mobiles Funduskop, ein Smartphone, und die eye2you Netzhautanalyse-KI. Dadurch sind Netzhautuntersuchungen günstiger, schneller und breiter verfügbar. Das hilft Sehkraft-gefährdende Krankheiten wie diabetische Retinopathie oder grünen Star zu erkennen bevor es zu spät ist: www.eye2you.ai.