Ergebnisse jetzt verfügbar: EU-MDR-Umfrage zum Stand der Umsetzung

DATUM
30. März 2020
AUTOR
Tereza | Senior Customer Success Manager
In Bezug auf die EU-MDR (Medizinprodukteverordnung 2017/745) herrschte in letzter Zeit eine große Unsicherheit. Mitten in der COVID-19-Pandemie und auf Forderung des BVMed hin hat die EU Kommission kürzlich die Empfehlung ausgesprochen, den MDR-Geltungsbeginn um 12 Monate zu verschieben. Der Mangel an Benannten Stellen (im März 2020 waren es 12) und die Tatsache, dass das Coronavirus erhebliche Engpässe im MedTech-Markt verursachen könnte (etwa wenn bestimmte Gerätezertifikate nicht rechtzeitig verlängert werden können), waren nur einige der Gründe für das geforderte Moratorium. Die Ergebnisse dieser EU-MDR-Umfrage zeigen, inwiefern MedTech-Unternehmen auf die EU-MDR vorbereitet waren.
Am 26. Februar 2020 wurde unsere MDR-Umfrage veröffentlicht, um den Stand der Umsetzung der neuen Anforderungen in Europa zu bewerten. Die Umfrage bestand aus 14 Fragen und wurde am 25. März 2020 abgeschlossen. 110 Unternehmen nahmen insgesamt teil, die meisten davon (85%) Medizinproduktehersteller. Obwohl Teilnehmer aus ganz Europa mitmachten, kam die Mehrheit (86%) aus dem deutschsprachigen Raum. Hier einige Ergebnisse im Überblick:
Die wichtigsten Ergebnisse in Kürze
- Mehr als drei Viertel (77%) schätzen die neue Verordnung als „sehr herausfordernd“ ein
- Zu den größten Herausforderungen zählen „Fehlende Klarheit“ sowie „Höherer Ressourcen- und Kostenaufwand“
- Rund ein Drittel glaubt, dass die EU-MDR mehr als 5% ihres Jahresumsatzes kosten wird
- Erst 26% haben ein vollständig MDR-konformes QMS
- 34% haben noch keine Benannte Stelle oder befinden sich gerade in der Wechselphase
- Knapp die Hälfte hat (noch) keinen PMS-Plan
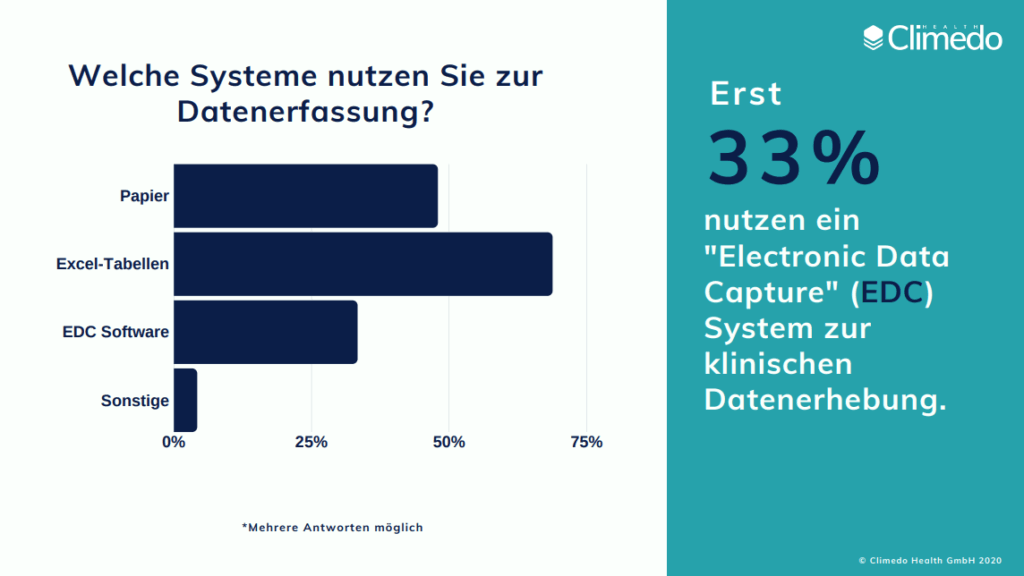
- 48% nutzen noch papierbasierte Systeme für die klinische Datenerfassung, 69% Excel-Tabellen (mehrere Nennungen möglich)
Wie geht’s weiter?
Insgesamt zeigen die Ergebnisse der EU-MDR-Umfrage, dass nur wenige Unternehmen hinsichtlich ihrer Post-Market-Überwachung (PMS), Qualitätsmanagementsysteme (QMS), Benannten Stellen und Datenerfassungssysteme auf die neue Verordnung vorbereitet waren. Wir sind gespannt darauf zu sehen, was der MedTech-Branche im kommenden Jahr bevorsteht und hoffen, dass Ihnen diese Auswertung ein paar neue Impulse bietet. Falls Sie Fragen oder Feedback haben, können Sie sich jederzeit an uns wenden: hello@climedo.de.
Update vom 6. April 2020. Wie Devicemed berichtet, hat die Europäische Kommission am Freitag, den 3. April 2020 das Proposal für die Verschiebung des MDR-Geltungsbeginns veröffentlicht.
Diesen Beitrag auf LinkedIn lesen.
In der Zwischenzeit könnten auch folgende Inhalte für Sie interessant sein:
Whitepaper: Mit digitalen Lösungen zu einer fundierten EU-MDR-Strategie
Slide Deck: 6 häufige PMCF-Fehler im Zuge der EU-MDR
Infografik: 5 Schritte zur Vorbereitung auf die EU-MDR
Whitepaper: PMS in der EU-MDR-Ära meistern
Playbook: Wie die EU-MDR die Zukunft der MedTech-Branche prägen wird