Umfrage zu den wahren Kosten der EU-MDR: Ein Zwischenstand

DATUM
11. August 2020
AUTOR
Benjamin Sauer | VP Engineering
Vor kurzem haben wir unsere EU-MDR-Umfrage zu den wahren Kosten der neuen Verordnung gestartet. Falls Sie oder Ihre Kunden von der neuen Verordnung betroffen sind und noch nicht teilgenommen haben, nehmen Sie sich doch ein paar Minuten Zeit, um dies nachzuholen! Die Ergebnisse teilen wir mit allen Interessenten, die ihre E-Mail-Adresse hinterlassen.
Nachdem wir schon über 80 Umfrageteilnehmer, darunter größtenteils Medizinproduktehersteller, gewinnen konnten, freuen wir uns, einen Teil der vorläufigen Ergebnisse mit Ihnen teilen zu können. Hierbei haben wir uns zunächst auf vier der 15 Fragen konzentriert:
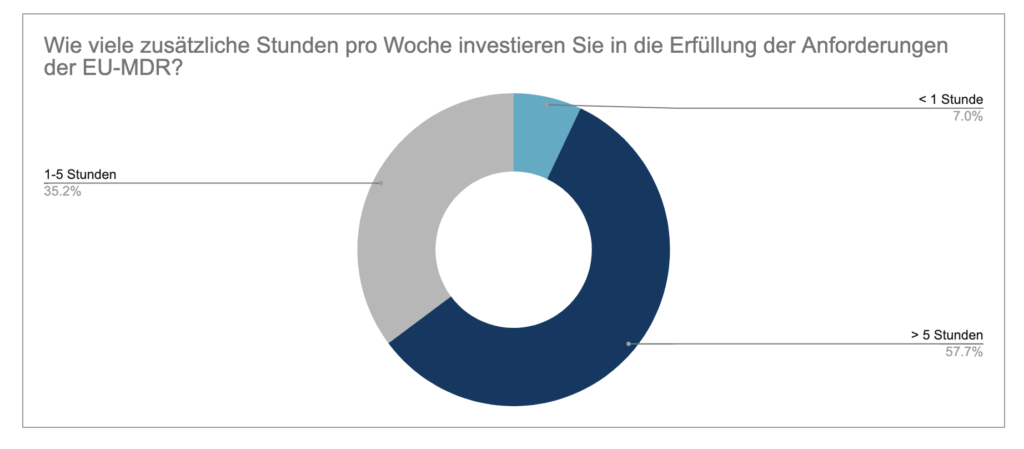
- Wie viele zusätzlichen Stunden pro Woche wird in die Erfüllung der EU-MDR-Anforderungen investiert?
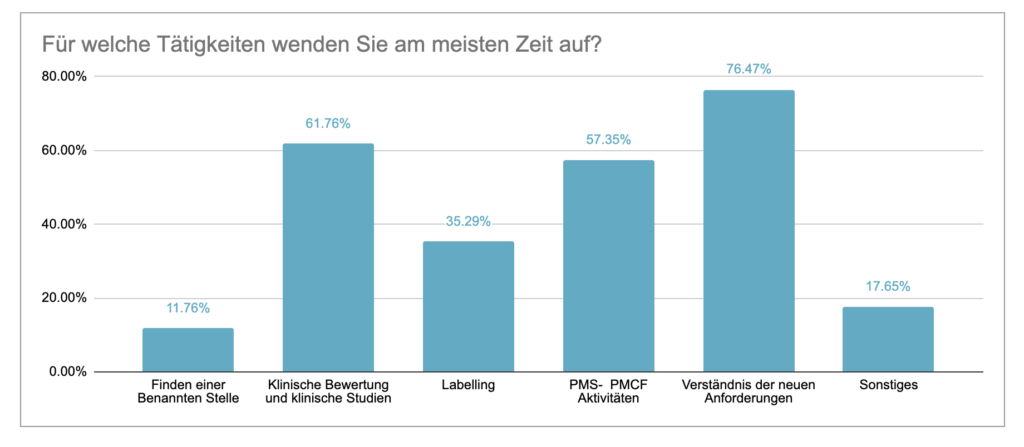
- Für welche Tätigkeiten wird am meisten Zeit aufgewendet?
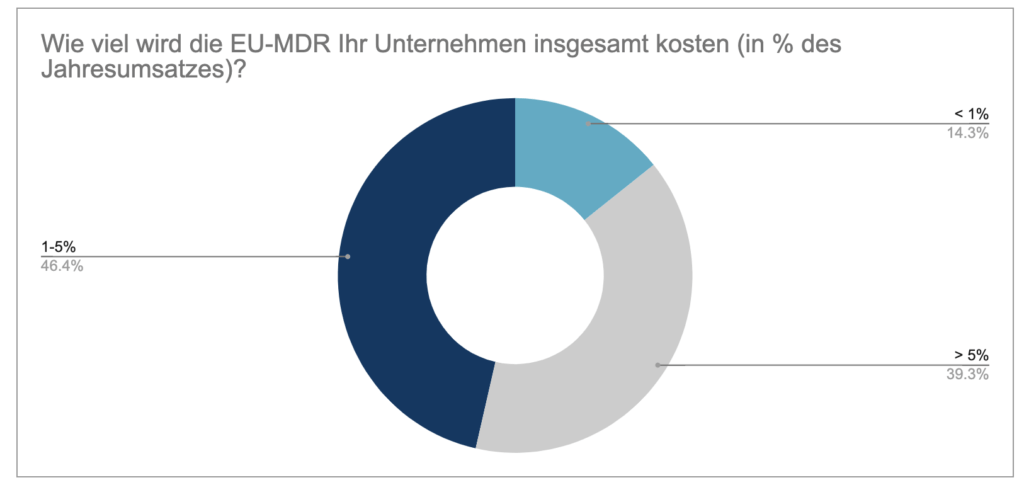
- Wie viel investieren Unternehmen insgesamt in die EU-MDR?
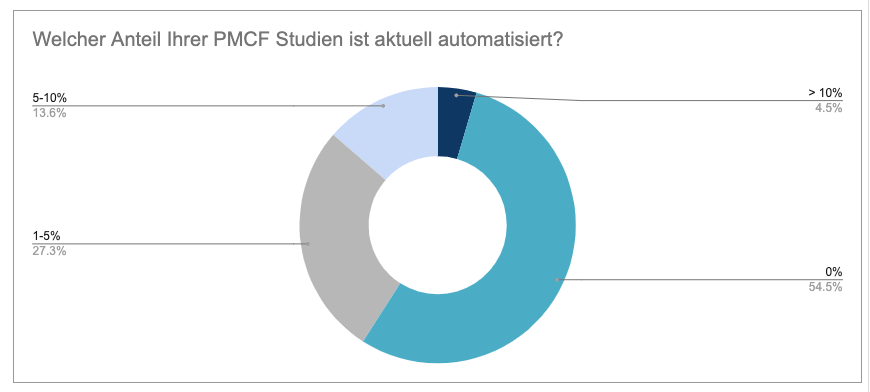
- Welcher Anteil von PMCF-Studien ist aktuell automatisiert?
Zeit ist Geld
Mehr als die Hälfte der bisherigen Teilnehmer (57%) geben an, mehr als 5 Stunden pro Woche in die Erfüllung der neuen Verordnung zu investieren. Über ein Drittel (35%) investieren 1 bis 5 Stunden pro Woche und nur 7% investieren weniger als eine Stunde.
Am meisten Zeit fließt in das Verständnis der Anforderungen
Für 76.5% der Teilnehmer ist unter anderem das Verständnis der neuen Anforderungen besonders zeitaufwendig. Zudem wurden vor allem klinische Bewertungen bzw. Klinische Studien (61.7%) sowie PMS- und PMCF-Aktivitäten (57.3%) genannt. Labelling und das Finden einer Benannten Stelle wurden etwas weniger genannt, mit je 35% und 11.7%. Zu sonstigen genannten Bereichen, in denen besonders viel Zeit investiert werden muss, zählen Gap-Analysen (MDD-MDR), die Auswahl harmonisierter Normen, der Aufbau eines QMS, Beratung und Konformitätserklärungen.
Die EU-MDR bleibt eine teure Angelegenheit
Zudem hat uns noch interessiert, welchen Anteil ihres Jahresumsatzes Medizinproduktehersteller aktuell in die Erfüllung der Anforderungen investieren müssen. Diese Frage haben wir bereits in unserer ersten Umfrage aus dem Frühjahr an Hersteller gestellt. Diesmal glaubten 46%, dass sie 1-5% ihres Umsatzes in die Bewältigung der Anforderungen investieren müssen und 39% glauben sogar, dass es mehr als 5% sein werden. Gerade mal 14% denken, dass es weniger als 1% sein wird. Zuvor glaubten 48%, dass sie 1-5% ihres Jahresumsatzes investieren müssten, 31,6% glaubten, dass es über 5% wären und 20,4% dachten, dass es weniger als 1% wären. Somit schätzen die Teilnehmer die Kosten mittlerweile sogar insgesamt höher ein als noch vor einigen Monaten.
Luft nach oben für die Automatisierung von PMCF-Studien
Ein weiterer Bereich, der uns bei Climedo besonders am Herzen liegt, ist die Automatisierung von PMCF-Studien im Rahmen der Post-Market-Überwachung. Mehr als die Hälfte der bisherigen Teilnehmer (54.5%) haben noch gar keine automatisierten Prozesse innerhalb ihrer PMCF-Aktivitäten. Doch immerhin haben 27.3% bereits einen kleinen Teil (1-5%) automatisiert, fast ein Viertel (13.6%) zwischen 5 und 10% automatisiert und einige wenige (4.5%) sogar schon mehr als 10% automatisiert. Dies ist ermutigend, doch gibt es beim Großteil der Hersteller ganz klar noch Luft nach oben. Gerade angesichts der EU-MDR wird es fast unmöglich sein, mit analogen Prozessen wie Papier oder Excel den Anforderungen gerecht zu werden. Mit automatisierten PMCF-Prozessen können zudem enorme Zeit und Kosten gespart werden.
Wie sieht es in Ihrem Unternehmen bzw. bei Ihren Kunden aus? Wir würden uns sehr freuen, wenn Sie kurz an unserer Umfrage teilnehmen würden. Die Ergebnisse erhalten Sie selbstverständlich kostenlos im Nachgang zugeschickt. Dazu müssen Sie lediglich Ihre E-Mail-Adresse hinterlassen.
Umfrage aus dem Frühjahr 2020: Stand der MDR-Umsetzung
Im Frühjahr führten wir eine erste Umfrage zum Stand der Umsetzung durch. Die Ergebnisse zeigten, dass viele MedTech-Unternehmen noch nicht auf die neuen Anforderungen vorbereitet waren und die Verschiebung der Geltungsfrist um 12 Monate mit Sicherheit eine Erleichterung gewesen sein wird. Hier finden Sie die Ergebnisse zum kostenlosen Download: