Medizinprodukte richtig klassifizieren – so funktioniert’s

DATUM
06. Februar 2020
AUTOR
Benjamin Sauer | VP Engineering
In der Europäischen Union (EU) sind Medizinprodukte in vier Hauptklassen unterteilt: I, IIa, IIb und III. Die Klassifizierung dieser Geräte beruht auf einem risikobasierten System, welches sich an der Verletzlichkeit des menschlichen Körpers und dem Risikopotenzial des Produkts orientiert. Dieses Risiko steigt von Klasse I bis Klasse III schrittweise an. Produkte der Klasse I bergen ein sehr geringes oder kein Risiko, während Produkte der Klasse III ein sehr hohes Risiko für Patienten darstellen. Mit der EU-MDR gibt es einige wichtige Änderungen des Klassifizierungssystems.
Generell wird empfohlen, die folgenden für die Technische Dokumentation notwendigen Dokumente (MDR Anhang II, 1.1) vor der Klassifizierung des Medizinprodukts zu erstellen:
(a) eine allgemeine Beschreibung des Produkts, einschließlich seiner Zweckbestimmung auf dem Markt sowie seiner vorgesehenen Anwender;
(c) die geplante Patientengruppe, der zu diagnostizierende/ behandelnde und/oder zu überwachenden medizinische Zustand, sowie andere Erwägungen wie Auswahlkriterien, Indikationen, Kontraindikationen und Warnhinweise;
(d) die Funktionsprinzipien des Gerätes und seine Wirkungsweise, falls erforderlich wissenschaftlich nachgewiesen
Whitepaper: From Data to Dialogue | Elevating Science-Based Communication in Post-Approval Studies
Unser Whitepaper zeigt auf, wie man nach der Zulassung einer Behandlung einen entscheidenden Vorteil erlangen kann. Hierbei legen wir einen besonderen Schwerpunkt auf nicht-interventionelle Studien (NIS). Dafür werden Strategien skizziert, mit denen man um Daten durch moderne digitale Lösungen in erfolgreiche Dialoge verwandelt.
Medizinprodukte der Klasse I
Produkte der Klasse I sind meist nicht-invasive Produkte, die keine Auswirkungen auf den menschlichen Körper haben und ein sehr geringes Risiko aufweisen. Klasse I Produkte unterliegen nicht der Zertifizierung durch Benannte Stellen („Notified Bodies“) und können vom Unternehmen selbst zertifiziert werden kann. Laut einer 2017 veröffentlichten Infografik des BVMED machen Geräte der Klasse I einschließlich der Unterklassen etwa 70% des Markts aus.
Klasse I enthält allerdings drei Unterklassen, für welche Hersteller zum Teil eine Benannte Stelle bei der Konformitätsbewertung einbinden müssen. Medizinprodukte, die in sterilem Zustand auf den Markt gebracht werden, werden als Klasse Is kategorisiert („s“ steht für das englische „sterile“). Produkte mit Messfunktion werden als Klasse Im bezeichnet („m“ steht für „measure„). Laut MDR-Gesetz gibt es zudem eine neue Unterklasse: Produkte, die wiederverwendet oder wiederaufbereitet werden können, werden als Klasse Ir (“r” steht für “reusable“) bezeichnet. Weitere nützliche Informationen hierzu finden Sie beim Johner Institut.
| Klassifizierung | Definition | Beispiele | Zertifizierung erforderlich? |
| Klasse I | Geräte, die nicht steril sind oder keine Messfunktion haben (geringes Risiko) | Rollstühle, Pflaster, Krankenhausbetten, Bettpfannen | Nein |
| Klasse Is | Produkte, die in sterilem Zustand auf den Markt gebracht werden | Schutzausrüstung | Teilweise |
| Klasse Im | Geräte mit Messfunktion | Stethoskope, Thermometer, Waagen | Teilweise |
| Klasse Ir | Eine neue Unterklasse für Produkte, die wiederaufbereitet oder wiederverwendet werden | Chirurgische Instrumente und Endoskope | Teilweise |
Für Produkte der Klasse I, die keine Zertifizierung durch eine Benannte Stelle erfordern, muss der Hersteller die Dokumente selbst erstellen und vorhalten.
Korrigendum: MDR-Fristverlängerung für Produkte der Klasse I
Für nun höhergestufte Produkte der Klasse I sieht ein im Dezember 2019 veröffentlichtes Korrigendum eine vierjährige Frist vor, bevor diese ein Zertifikat von einer im Rahmen der MDR ernannten Benannten Stelle erhalten müssen. Dies mildert zumindest für einige Hersteller von Klasse I Produkten die Schwierigkeiten bei der Anwendung der neuen Vorschriften. Die Übergangsfristen für MDD/AIMDD-konforme Geräte beziehen sich jedoch nur auf die Zertifizierungsanforderungen. Andere Verpflichtungen für diese Produkte – wie z.B. Risiko- und Qualitätsmanagement oder Anforderungen an die klinische Bewertung – treten am 26. Mai 2021 in Kraft.
Digitale Gesundheitsanwendungen
Digitale Gesundheitsanwendungen (kurz “DiGA”) sind sind Medizinprodukte niedriger Risikoklasse (I bis IIa), die dazu bestimmt sein müssen:
- Krankheiten zu erkennen, zu überwachen, zu behandeln oder zu lindern
- Bzw. Verletzungen oder Behinderungen zu erkennen, zu behandeln, zu lindern oder zu kompensieren.
Sollte Ihr Produkt in die DiGA-Kategorie fallen, können Sie sich hier informieren.
Medizinprodukte der Klasse II
Die nächste Risikoklasse bilden Klasse II-Produkte, die in die Unterklassen IIa und IIb unterteilt sind. Produkte der Klasse IIa bergen ein mittleres Risiko und Produkte der Klasse IIb ein mittleres bis hohes Risiko. Um ein Medizinprodukt der Klasse IIa oder IIb mit der CE-Kennzeichnung zu versehen und auf den Markt zu bringen, müssen die Hersteller über eine Benannte Stelle verfügen. Diese stellt nach Prüfung der Konformität mit den in der Verordnung festgelegten Verfahren ein CE-Zertifikat aus.
Klasse IIa
Diese Produkte werden oft mithilfe einer externen Energiequelle betrieben oder zur Diagnose oder Überwachung von Krankheiten eingesetzt. Nach Angaben des BVMED machen sie 20% des Markts aus. Produkte der Klasse IIa sind generell invasiv, allerdings sind sie auf natürliche Körperöffnungen beschränkt. Falls diese Produkte in irgendeiner Weise potenziell gefährlich für einen Patienten sind, werden sie automatisch der Klasse IIb zugeordnet.
Klasse IIb
Die Klasse IIb beinhaltet die meisten chirurgisch-invasiven oder aktiven Produkte, die teilweise oder vollständig in den Körper eingesetzt werden. Produkte dieser Klasse können auch die Zusammensetzung von Körperflüssigkeiten verändern. Sie machen nach Angaben des BVMED 8% des Markts aus.
| Klassifizierung | Definition | Beispiele | Zertifizierung erforderlich? |
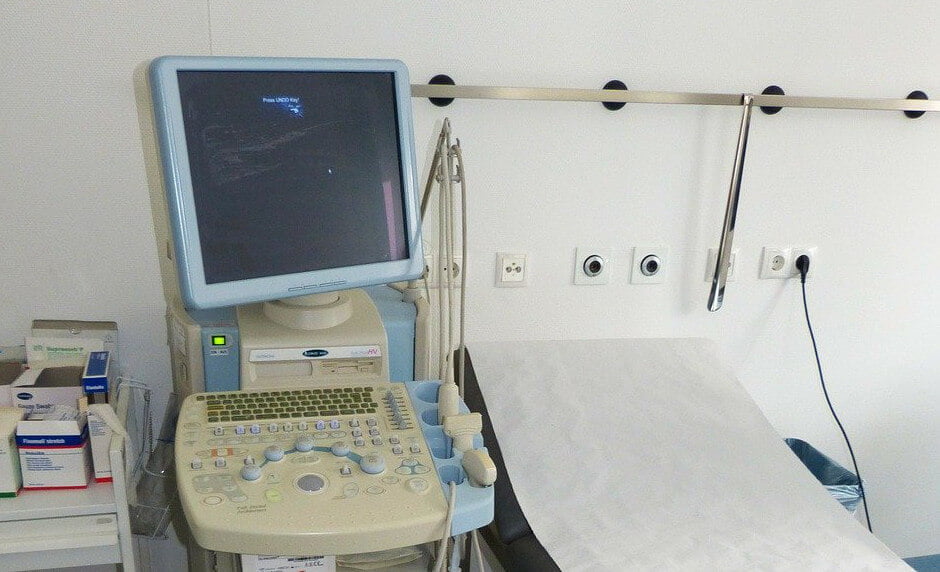
| IIa | Geräte, die kurzfristig (in der Regel 60 Minuten bis 30 Tage) in den Körper eingesetzt werden | Hörgeräte, Ultraschall-Diagnosegeräte, Katheter | Ja |
| IIb | Geräte, die etwas komplexer als IIa-Geräte sind und oft für mehr als 30 Tage im Körper eingesetzt werden. | Infusionspumpen, Beatmungsgeräte, chirurgische Laser, Geräte für Intensivüberwachung, Zahnimplantate | Ja |
Medizinprodukte der Klasse III
Abschließend werden Produkte mit dem höchsten Risiko für Patienten in die Klasse III eingestuft. Diese Produkte haben entweder lebenserhaltende Funktionen und sind somit von erheblicher Bedeutung für die menschliche Gesundheit oder stellen ein besonders hohes methodisches Krankheits- oder Verletzungsrisiko dar. Um die Sicherheit und Wirksamkeit dieser Produkte zu gewährleisten, ist eine wissenschaftlichen Überprüfung vor dem Inverkehrbringen für die Zulassung erforderlich.
| Klassifizierung | Definition | Beispiele | Zertifizierung erforderlich? |
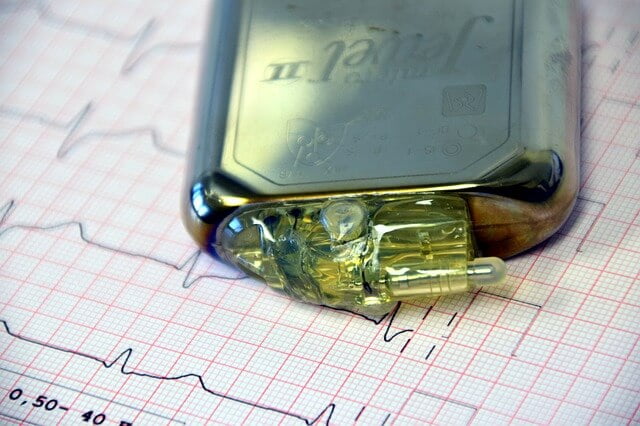
| Klasse III | Geräte, die unmittelbar am zentralen Kreislauf- oder Nervensystem eingesetzt werden oder ein Medikament enthalten. | Herzschrittmacher, prothetische Herzklappe | Ja |
Die Bestimmung der richtigen Risikoklasse eines Produkts kann eine Herausforderung sein, insbesondere wenn es um die Zertifizierung und Zulassung geht. Wir empfehlen, jedes Produkt einzeln zu betrachten und zu beurteilen. Darüber hinaus kann es hilfreich sein, einen autorisierten Vertreter zu kontaktieren oder in den Klassifizierungsregeln nachzuschauen. Im Rahmen des MDR-Gesetzes gibt es vier neue Regeln für die Klassifizierung, die sie hier finden können.
Möchten Sie mehr über die EU-MDR und die Automatisierung Ihrer Post-Market Surveillance (PMS) und Post-Market Clinical Follow-up (PMCF) Aktivitäten erfahren? Vereinbaren Sie jetzt eine Demo mit uns.
Weitere EU-MDR-Inhalte
Umfrageergebnisse: Die wahren Kosten der EU-MDR
Whitepaper: Mit digitalen Lösungen zu einer fundierten EU-MDR-Strategie
Playbook: Wie die EU-MDR die Zukunft der MedTech-Branche prägen wird